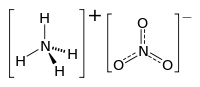
Nitrato d'ammonio
| Nitrato d'ammonio | |
|---|---|
| Nome IUPAC | |
| Triossonitrato di ammonio | |
| Caratteristiche generali | |
| Formula bruta o molecolare | NH4NO3 |
| Peso formula (u) | 80,0432 |
| Aspetto | solido incolore |
| Numero CAS | |
| Numero EINECS | 229-347-8 |
| PubChem | 22985 |
| SMILES | [NH4+].[N+](=O)([O-])[O-] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,72 |
| Solubilità in acqua | 1180 g/L (0 °C) 1920 g/L (20 °C) 4100 g/L (60 °C) 10240 g/L (100 °C)[1] |
| Temperatura di fusione | 169 °C (442 K) |
| Temperatura di ebollizione | decomposizione a 210 °C (483 K) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −365,6 |
| ΔfG0 (kJ·mol−1) | −183,9 |
| S0m(J·K−1mol−1) | 151,1 |
| C0p,m(J·K−1mol−1) | 139,3 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 272 |
| Consigli P | 210 [2] |
Il nitrato d'ammonio è un composto chimico che viene utilizzato come fertilizzante, ma anche per produrre l'ammonal e l'ANFO, due esplosivi. È il componente attivo del cosiddetto "ghiaccio istantaneo".
Caratteristiche
È il sale dell'ammoniaca con l'acido nitrico. La sua formula chimica è NH4NO3.
Si presenta in forma di cristalli incolori e inodori. È molto solubile in acqua (1920 g/L a 20 °C) e mediamente solubile in etanolo (38 g/L a 20 °C).
Una soluzione di 100 g/L in acqua ha un pH di 5,5, lievemente acido.
Il composto è stabile a temperature ordinarie, se riscaldato progressivamente all'interno di una provetta su becco Bunsen svolge N2O (protossido d'azoto, gas esilarante) più NO e NO2 come sottoprodotti.
A temperature attorno a 300 °C, la decomposizione produce principalmente protossido d'azoto e acqua:
A temperature superiori prevale invece questa reazione
Entrambe le reazioni sono esotermiche e producono composti gassosi. In determinate condizioni questo può produrre una reazione a catena in cui la decomposizione diventa esplosiva.
Utilizzi
Fertilizzante
È uno dei più importanti composti azotati usati come concimi nell'agricoltura. La sua peculiarità sta nel fatto che contiene sia azoto immediatamente utilizzabile da parte della pianta (gruppo nitrato), sia azoto a lento rilascio (gruppo ammoniacale). Il suo tenore NPK è 33-0-0.
Ghiaccio istantaneo
Reagisce endotermicamente con l'acqua, il che lo rende il componente attivo del cosiddetto "ghiaccio istantaneo", per uso medico o sportivo.
Esplosivo
Dato il suo bilancio di ossigeno positivo e il costo poco elevato, costituisce la base per numerose miscele esplosive; inoltre la sua bassissima sensibilità all'innesco rende gli esplosivi che lo contengono adatti a usi civili o dove sia richiesta una grande sicurezza d'uso. Dà luogo ad un'esplosione relativamente poco esotermica e questo rende il loro utilizzo sicuro nelle miniere, in quanto il calore liberato nell'esplosione non è sufficiente ad innescare un'eventuale fuoriuscita di gas "grisù".
Il fatto di essere economico, sicuro e di facilissima reperibilità, lo ha reso noto come uno dei prodotti preferiti da organizzazioni terroristiche per la fabbricazione di ordigni, e per questo motivo la sua commercializzazione è stata compiutamente disciplinata dai Regolamenti CE 2003/2003 e 552/2009, nei quali sono state inserite prove di detonabilità.
Incidenti
Il nitrato d'ammonio è stato la causa di alcuni grandi disastri industriali.
- Il disastro di Halifax del 6 dicembre 1917 che uccise quasi 2000 persone e la cui potenza di circa 2,9 kilotoni fu la più potente esplosione di origine artificiale prima dell'utilizzo della bomba atomica.
- Il disastro di Texas City il 16 aprile 1947, dove un'esplosione pari a circa 3,8 kilotoni, l'equivalente di una piccola testata nucleare, uccise non meno di 581 persone.
- Le esplosioni al porto di Tientsin del 12 agosto 2015 che uccisero 173 persone e di cui la seconda e più potente era dovuta a 800 tonnellate di nitrato d'ammonio, pari a 0,336 kilotoni[3].
- Il 4 agosto 2020 un incendio di origine sconosciuta scoppiato nel porto di Beirut ha innescato un'enorme esplosione di 2750 tonnellate di materiale depositato, pari a 1,1 kilotoni.[4] L'onda d'urto conseguita ha provocato almeno 135 morti, ingenti danni alla città e alla popolazione.[5]
Note
- ^ (EN) Process of producing concentrated solution of ammonium nitrate
- ^ (EN) Ammonium nitrate, in GESTIS Substance Database, IFA - Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. URL consultato il 19 maggio 2020 (archiviato dall'url originale l'11 novembre 2016).
- ^ (EN) Ping Huang e Jingyuan Zhang, Facts related to August 12, 2015 explosion accident in Tianjin, China, in Process Safety Progress, vol. 34, n. 4, 2015, pp. 313–314, DOI:10.1002/prs.11789.
- ^ Jonathan Amos e Paul Rincon, Beirut blast was 'historically' powerful, BBC, 5 ottobre 2020.
- ^ Beirut, esplosioni al porto, più di 135 morti e 5 mila feriti, Rai news, 5 agosto 2020.
Voci correlate
Altri progetti
 Wikimedia Commons contiene immagini o altri file su nitrato d'ammonio
Wikimedia Commons contiene immagini o altri file su nitrato d'ammonio
Collegamenti esterni
- (EN) Nitrato d'ammonio, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 37241 · NDL (EN, JA) 00576059 |
|---|
Informazione
L'articolo Nitrato d'ammonio in Wikipedia italiana ha preso i seguenti posti nella classifica di popolarità locale:
- 1 ° posto il 2020-08-04
- 1 ° posto il 2020-08-05
- 2 ° posto il 2020-08-06
- 2 ° posto il 2020-08-07
- 19 ° posto il 2020-08-08
- 60 ° posto il 2020-08-09
Sulla pagina
Il contenuto presentato dell'articolo di Wikipedia è stato estratto 2021-06-13 sulla base di https://it.wikipedia.org/?curid=56008